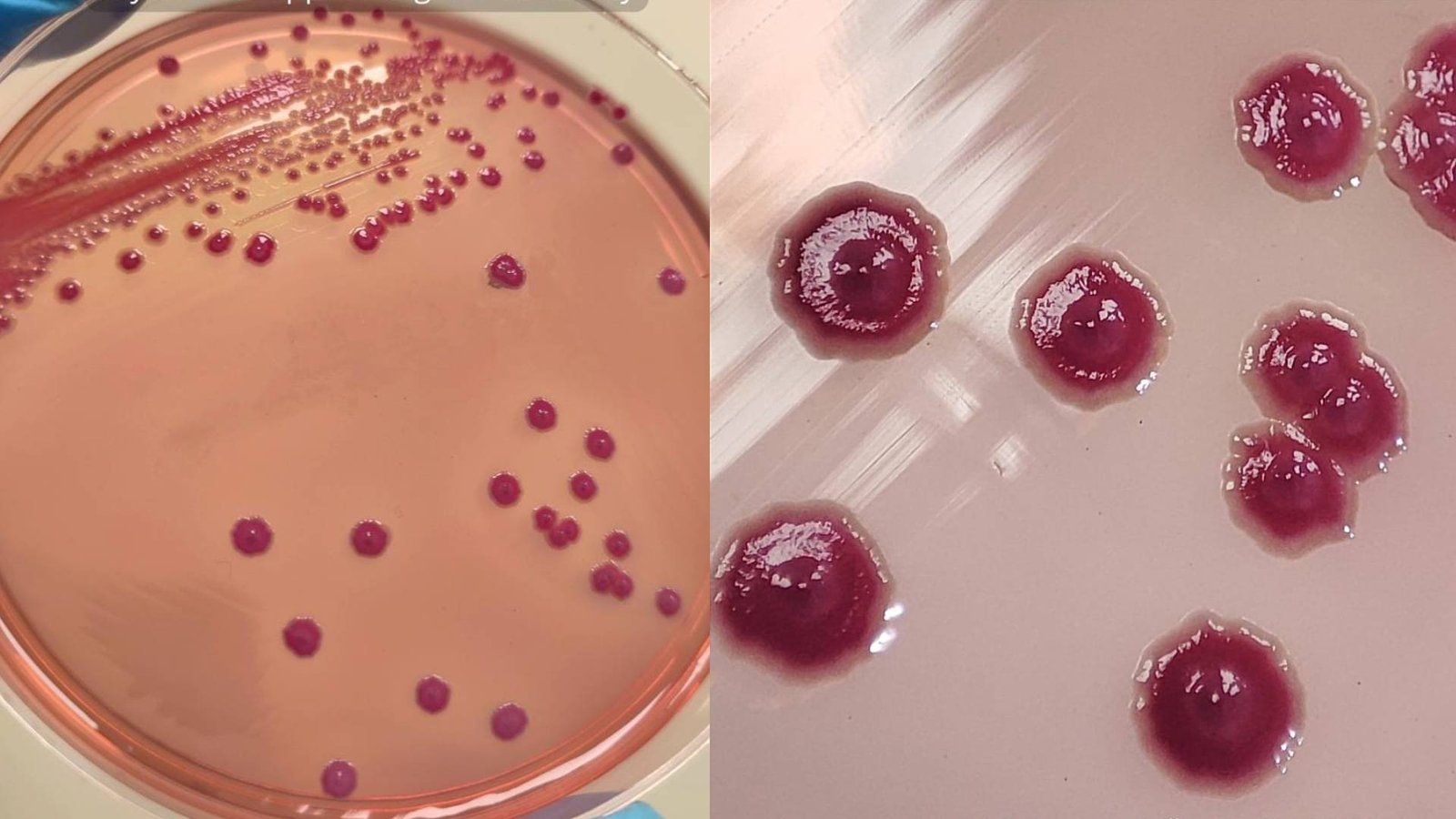
Em 2013, o Brasil testemunhou um alarmante surto de sepse que acometeu 65 recém-nascidos, resultando na morte trágica de 15 bebês prematuros. Esse episódio lamentável, ocorrido em unidades hospitalares, expôs a presença de uma Bactéria Phytobacter diazotrophicus, um microrganismo emergente e particularmente desafiador de identificar. Mesmo uma década após o surto, essa bactéria continua a ser confundida com outras espécies em exames laboratoriais, tanto no Brasil quanto globalmente, segundo alertas de especialistas.
A dificuldade reside na natureza elusiva da *Phytobacter diazotrophicus*. Conforme explicou o microbiologista brasileiro Marcelo Pillonetto, sistemas automatizados de identificação e testes bioquímicos, frequentemente empregados em laboratórios, falham em distinguir corretamente a *Phytobacter* de outros gêneros próximos. Comummente, a espécie é erroneamente categorizada como *Pantoea*, mas a confusão se estende a outros “parentes” próximos, como *Enterobacter*, *Kluyvera* e *Citrobacter*.
Bactéria Phytobacter diazotrophicus: desafio no diagnóstico persiste
Essa narrativa da descoberta e dos desafios persistentes é recontada no documentário “A Saga do Phytobacter”, lançado neste ano e financiado pela Secretaria de Estado da Ciência, Tecnologia e Ensino Superior (Seti) do estado do Paraná. O trabalho documenta a jornada para entender um patógeno que se “disfarça” e levanta questões sobre a adequação dos métodos diagnósticos atuais.
Origem e Alcance do Surto de 2013
O surto inicial ocorreu entre outubro de 2013 e maio de 2014, atingindo quatro estados brasileiros: Paraná, Minas Gerais, São Paulo e Rio Grande do Sul. A contaminação foi associada à nutrição parenteral utilizada em terapias intravenosas hospitalares, que servia como meio para a proliferação bacteriana. Inicialmente, as análises de amostras clínicas apontavam para a presença da bactéria *Pantoea*. No entanto, investigações mais aprofundadas revelaram que o verdadeiro culpado era a *Phytobacter diazotrophicus*, marcando o primeiro registro documentado de infecção por essa espécie em seres humanos.
A correção dessa identificação taxonômica inadequada foi fruto de uma investigação científica rigorosa, liderada por Marcelo Pillonetto. A pesquisa, realizada pelo Laboratório Central do Paraná (Lacen/PR) – parte integrante do Sistema Único de Saúde (SUS) – em colaboração com a Universidade de Ciências Aplicadas de Zurique (ZHAW), utilizou testes avançados para desvendar a verdadeira natureza do microrganismo.
Originalmente descrita na China em 2008, onde foi isolada em plantações de arroz, a *Phytobacter diazotrophicus* só teve sua capacidade patogênica em humanos confirmada após os estudos detalhados no Brasil. A persistente confusão entre espécies, conforme detalhado por Pillonetto, deve-se à ineficácia dos métodos tradicionais e de muitos equipamentos automatizados de rotina em hospitais para diferenciar o *Phytobacter* de seus semelhantes.
Descobertas subsequentes revelaram que até mesmo genomas bacterianos depositados em bancos de dados internacionais, usados como referência global, estavam com nomes incorretos desde 1974. A retificação dessas informações foi comunicada oficialmente em 2018, e esforços foram feitos para atualizar os equipamentos laboratoriais. Em 2023, a espécie foi finalmente incluída no banco de dados de um fabricante de espectrometria de massa, um método mais moderno e rápido para a identificação bacteriana.
Reincidência e Novos Desafios no Diagnóstico
Apesar dos avanços, o desafio na identificação da bactéria permanece. Em 2023, um surto de menor proporção da mesma bactéria ocorreu em uma clínica de hemodiálise em São José dos Pinhais, na região metropolitana de Curitiba. Quatro pacientes desenvolveram sepse, mas felizmente todos sobreviveram, evidenciando a necessidade contínua de vigilância e aprimoramento diagnóstico.
Pillonetto ressalta que a identificação precisa da bactéria desencadeou um alerta na comunidade microbiológica, levando à distribuição de amostras para cerca de 300 laboratórios no Brasil e no exterior. O objetivo é capacitar os profissionais de saúde a reconhecerem esse “novo inimigo” invisível. Essa pesquisa evidencia um patógeno emergente, que tem sido confundido com diversas outras espécies. Um diagnóstico exato e rápido, seguido pela escolha do antibiótico adequado, é fundamental em infecções generalizadas, mas o desconhecimento ainda é uma barreira.
Estudos indicam que bactérias do gênero *Phytobacter* podem ser identificadas incorretamente com frequência em amostras clínicas. Essa confusão taxonômica dificulta o reconhecimento de surtos hospitalares e pode levar à subnotificação da presença dessas bactérias, cuja disseminação em ambientes hospitalares, por meio de soluções contaminadas ou superfícies, é preocupante, segundo Pillonetto.
Tecnologias de Identificação: Limitações e o Padrão Ouro
Quando os hospitais necessitam de uma identificação bacteriana em exames, os sistemas automatizados comuns na maioria dos laboratórios frequentemente falham em espécies complexas e emergentes. Embora esses aparelhos possuam bancos de dados extensos com bactérias conhecidas, a identificação de microrganismos novos ou incomuns exige o “padrão ouro” da microbiologia: o sequenciamento genético.

Imagem: g1.globo.com
O sequenciamento genético pode reduzir o tempo de identificação de aproximadamente 72 horas para apenas 24 horas, além de revelar modificações na bactéria e seu perfil de resistência, o que otimiza a seleção de antibióticos. No entanto, essa tecnologia ainda é de acesso limitado, restrita a laboratórios de pesquisa e hospitais privados de alta complexidade. A razão reside nos altos custos dos kits de sequenciamento, importados e sobrecarregados por impostos elevados.
O professor Nilton Lincopan, do Departamento de Microbiologia do ICB-USP, salienta que as ferramentas genômicas são dispendiosas e requerem mão de obra altamente qualificada. Contudo, são indispensáveis para identificar bactérias emergentes. Ele sugere uma alternativa: fortalecer a colaboração entre laboratórios públicos, hospitais e centros de pesquisa universitários. Um exemplo da onerosidade é o custo de R$ 75 mil para um kit adquirido por sua equipe, capaz de sequenciar 96 bactérias. Após aberto, o material tem validade limitada, o que exige o acúmulo de amostras e pode, paradoxalmente, atrasar os diagnósticos. Kits menores (para 24 bactérias) existem, mas sua disponibilidade é irregular.
Lincopan sugere que “laboratórios-escola” universitários poderiam servir como referência regional, evitando que o sistema público de saúde arcasse com os custos de infraestrutura e pessoal qualificado, ao mesmo tempo em que cumpririam sua função de extensão universitária. Essa integração permitiria transformar dados científicos em pesquisa aplicada, crucial para enfrentar desafios como a resistência bacteriana, surtos hospitalares e diagnósticos precoces.
Marcelo Pillonetto reforça a importância vital da identificação precisa do *Phytobacter*, devido à sua crescente capacidade de adquirir genes de resistência a antibióticos potentes. Para o especialista, as instituições devem investir em equipamentos adequados e na capacitação de profissionais para aprimorar a identificação microbiológica, minimizar erros diagnósticos e combater a resistência antimicrobiana, um desafio global de saúde pública.
Casos e Potencial de Resistência
Inicialmente, as bactérias causadoras do surto de 2013 foram classificadas de forma diversa, incluindo *Acinetobacter baumannii*, *Rhizobium radiobacter* e *Pantoea*. Análises moleculares minuciosas, contudo, demonstraram que uma parte significativa dos isolados era, de fato, *Phytobacter diazotrophicus*. Os estudos confirmaram a presença de três bactérias principais no surto: *Acinetobacter baumannii*, *Phytobacter diazotrophicus* e *Rhizobium radiobacter*. As análises genéticas apontaram semelhança entre as duas primeiras, sugerindo uma fonte de contaminação comum, e em um dos pacientes, as três espécies foram detectadas simultaneamente.
Estudos internacionais confirmam a presença de espécies do gênero *Phytobacter* em ambientes hospitalares. Em Singapura, pesquisadores detectaram *Phytobacter diazotrophicus* em uma UTI neonatal, em amostras de torneiras e sifões de pia, inicialmente identificadas incorretamente como *Cronobacter sakazakii* e *Klebsiella oxytoca*, e confirmadas apenas por sequenciamento genético completo. Essas bactérias, presentes tanto em ambientes naturais quanto clínicos, têm sido cada vez mais relatadas em infecções humanas.
Pesquisas evidenciam ainda que algumas espécies de *Phytobacter* possuem genes de resistência a antibióticos de última geração. Um estudo na revista “Microbiology Spectrum” identificou *Phytobacter diazotrophicus* em pacientes pediátricos e ambientes hospitalares no Japão, com amostras contendo o gene blaNDM-1, associado à resistência a carbapenêmicos. Outro estudo reportou genes de resistência à colistina e à produção de carbapenemase, intensificando a preocupação com o potencial patogênico desse microrganismo. Além dos surtos hospitalares, há registros de infecções isoladas, como um caso de sepse por *Phytobacter ursingii* em uma paciente idosa com nutrição venosa e sepse neonatal na China por *Phytobacter diazotrophicus* em uma bebê de 27 dias com galactosemia tipo 1. O *Phytobacter* é reconhecido como patógeno oportunista, isolado em sangue humano, fluidos intravenosos e esgoto hospitalar.
Confira também: Imoveis em Rio das Ostras
O surto de 2013 no Brasil e a identificação precisa da *Phytobacter diazotrophicus* servem como um lembrete crítico para a necessidade de constante atualização nos laboratórios clínicos, na formação de profissionais e no investimento em tecnologia. É crucial que a atenção a esses patógenos emergentes seja redobrada, pois a acurácia diagnóstica é a linha de frente contra a disseminação e a resistência a tratamentos que podem salvar vidas. Acompanhe a editoria de Análises para mais discussões aprofundadas sobre desafios científicos e de saúde pública que impactam o Brasil.
Créditos das imagens: Laboratório Central do Paraná (Lacen/PR) e Nilton Lincopan